实现体内微观生物靶标(如亚百微米级的“休眠”肿瘤细胞簇)的高分辨率成像是疾病早期诊断和干预的终极目标。肿瘤细胞簇是导致癌症转移的“元凶”,但它们在体内往往处于休眠状态,难以被察觉。
传统的成像技术面临着不可调和的矛盾:PET和SPECT存在辐射且解剖分辨率不足;光学成像虽然分辨率高,但穿透深度有限,难以探测深部肿瘤。超高场磁共振成像(UHF MRI,≥7 T)凭借极高的空间分辨率和深层组织穿透力被寄予厚望。然而,现有的MRI造影剂(无论是传统金属螯合物还是纳米颗粒)在水分子配位能力上存在瓶颈,导致其纵向弛豫率(r1)不足,无法在超高场下提供足够的对比度来“点亮”这些微小的肿瘤细胞簇。
一种全新的“亲电性工程化磁性传感器(EEMS)”策略,通过引入高电负性金属原子,重塑了造影剂与水分子之间的磁性相互作用,成功打破了这一僵局。在这场“微观肿瘤追踪战”中,多场强核磁共振技术(涵盖0.5T低场弛豫分析至9T超高场成像)成为了见证造影剂性能飞跃的“关键裁判”。
研究团队从探针合成、弛豫性能、体外细胞检测到体内淋巴结转移追踪,对新型EEMS造影剂进行了系统评价,核心发现如下:
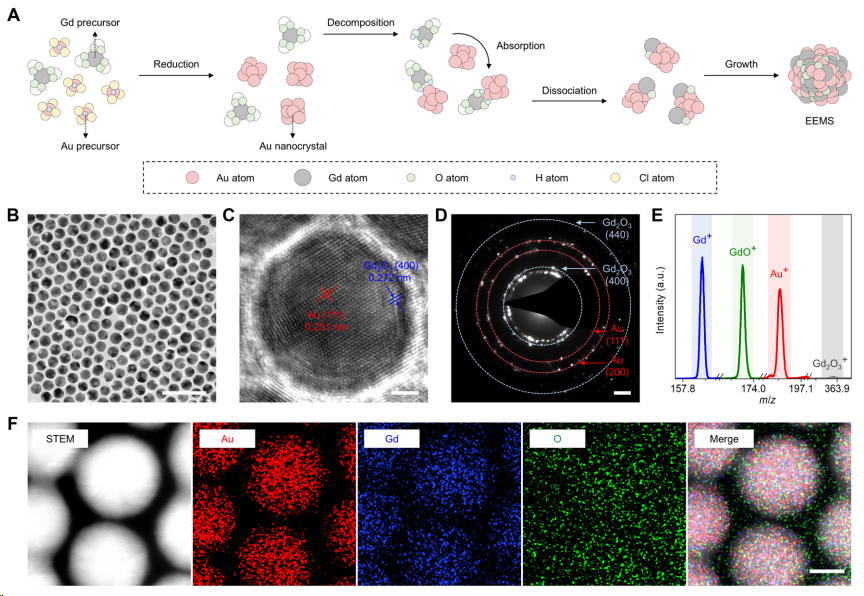
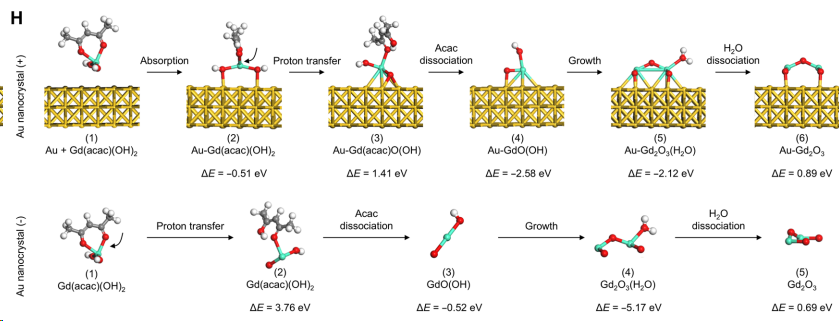
图注:EEMS合成机制、微观形貌与元素分布[包含A(合成示意图), B(TEM图), F(元素映射图), H(合成机制)]
核心机制: 传统纳米造影剂表面的配体往往会阻碍水分子的靠近。研究团队巧妙地将高电负性的金(Au)原子与钆(Gd)原子结合,合成了尺寸约12 nm的均一双金属纳米颗粒(EEMS)。Au原子的强吸电子能力显著增强了表面Gd原子的亲电性,使其能够像“磁铁”一样强烈吸引水分子中的富电子氧原子。
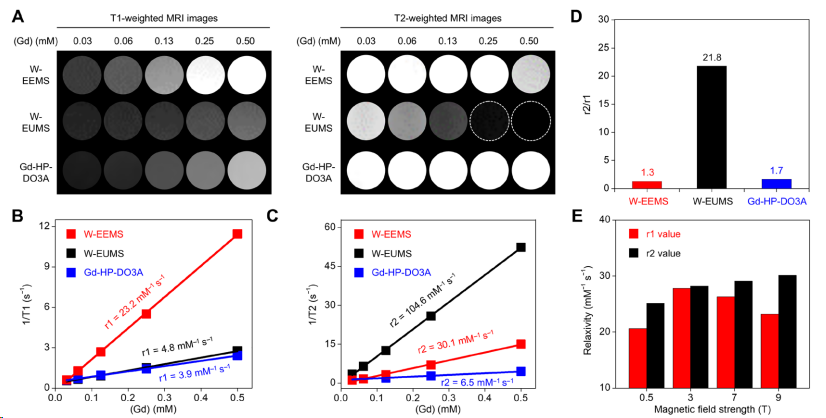
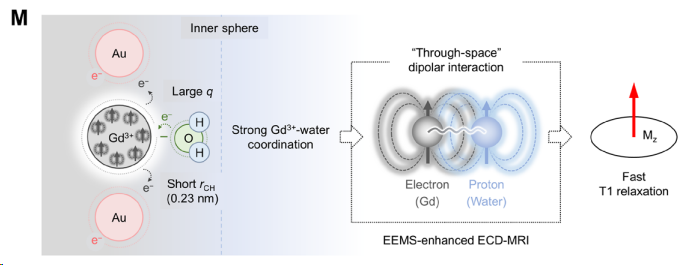
图注:EEMS在不同场强下的优异成像性能及ECD弛豫机制[包含 A(MRI成像对比图), B(r1曲线), E(不同场强下的弛豫率柱状图), M(ECD机制示意图)]
这是本研究最具突破性的部分。通过核磁共振弛豫分析,团队发现:
性能碾压: 在9T超高场下,EEMS的纵向弛豫率(r1)高达 23.2 mM⁻¹ s⁻¹,是临床常用造影剂(Gd – HP – DO3A)的近6倍!
机制揭秘(ECD原理): 这种性能飞跃得益于亲电催化偶极 – 偶极(ECD)相互作用。增强的亲电性缩短了Gd与水分子之间的配位距离(rCH < 0.23 nm),增加了内层配位水分子数量(q值),从而实现了极其高效的T1弛豫。
首次提出“ECD – MRI”造影机制:突破了传统SBM理论的限制,通过调节原子电负性(引入Au原子)来增强顺磁中心的亲电性,为开发下一代高性能MRI造影剂提供了全新的化学设计范式。
刷新活体检测分辨率极限:将活体肿瘤病灶的MRI检测极限推进至亚百微米级(<100 μm),填补了深部微小病灶无创高分辨成像的技术空白。
极高的临床转化价值:该探针不仅具有优异的生物相容性,还能在肿瘤转移的“休眠期”进行精准拦截,通过影像引导手术彻底切除隐患,为癌症的早期干预和预后改善提供了极具潜力的临床方案。
总结:核磁共振数据证明了——最好的造影剂,是能从原子层面“操控”水分子的造影剂。EEMS之所以胜出,正是因为它重塑了水分子与金属中心的磁性对话。
LF-NMR Equipment: NM20-060H-I, Niumag Analytical Instrument Co., Suzhou, China

文献来源:
Zeyu Liang, et al. An electrophilicity – engineered magnetic sensor for MRI detection of dormant tumor cell clusters. Science Advances, 12, eaea5236 (2026). DOI: 10.1126/sciadv.aea5236
电话:400-060-3233
售后:400-060-3233


返回顶部