磁共振成像(MRI)是临床诊断的重要工具,但目前广泛使用的造影剂几乎都依赖重金属(如钆Gd、锰Mn、铁Fe),存在潜在的毒性风险和组织沉积隐患。
为了寻找安全的替代品,科学家们致力于开发非金属造影剂(如有机自由基)。这类造影剂依靠未成对电子产生对比度,但面临一个致命痛点:体内稳定性极差。一旦进入人体,它们极易被体内的自由基清除途径“消灭”,导致造影能力瞬间失效(“见光死”)。
共轭聚合物(如聚吡咯 PPy)内部存在极其稳定的未成对电子(极化子),在体内具有极高的稳定性。然而,天然的PPy却无法直接用作造影剂,因为其内部强烈的“自旋 – 自旋”相互作用像一堵墙,阻挡了水分子质子的靠近,导致其T2造影能力极弱(处于“休眠”状态)。如何“唤醒”它?复旦大学邵正中教授团队给出了完美答案。
研究团队独辟蹊径,提出了一种“部分络合(Partially complexed)”策略,成功激活了PPy纳米颗粒的T2核磁造影性能。
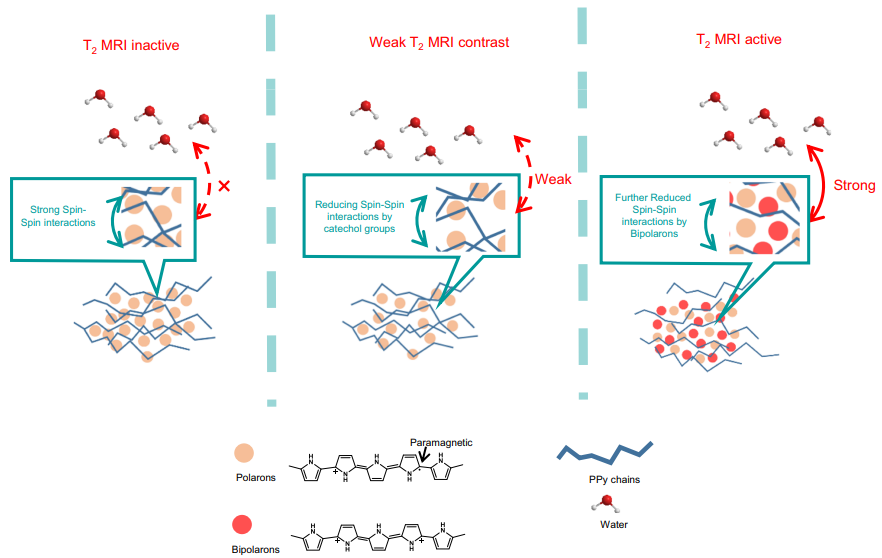
图注:[ Fig. 1:Schematic illustration (机制示意图)]天然PPy纳米颗粒因强相互作用阻挡水分子;通过“部分络合”法,儿茶酚衍生物适度削弱了该作用,成功“唤醒”了PPy的T2核磁造影性能。
研究人员引入了儿茶酚衍生物(如DHBA),将其与PPy结合。儿茶酚衍生物能够适度削弱PPy内部极化子之间的强相互作用。这一巧妙的“松绑”,让周围的水分子得以靠近顺磁中心,从而成功激活了其T2造影能力。
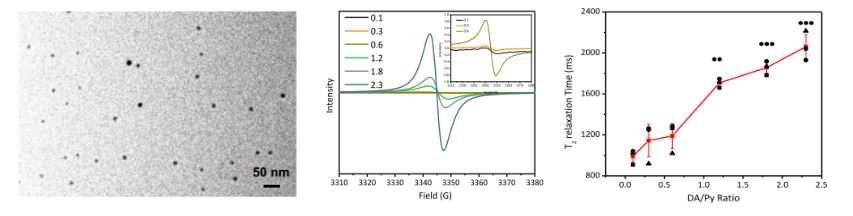
图注:[ Fig. 2:包含 TEM形貌图、ESR谱图 以及 T2弛豫时间拟合图]Catechol – PPy纳米颗粒的微观形貌、电子自旋共振(ESR)信号变化以及显著缩短的T2弛豫时间。
通过电子自旋共振(ESR)波谱分析,团队证实了改性后极化子状态的显著改变。更关键的是,在低场核磁测试中,改性后的Catechol – PPy纳米颗粒展现出了优异的横向弛豫性能,证明其已具备成为优秀T2造影剂的物理底子。
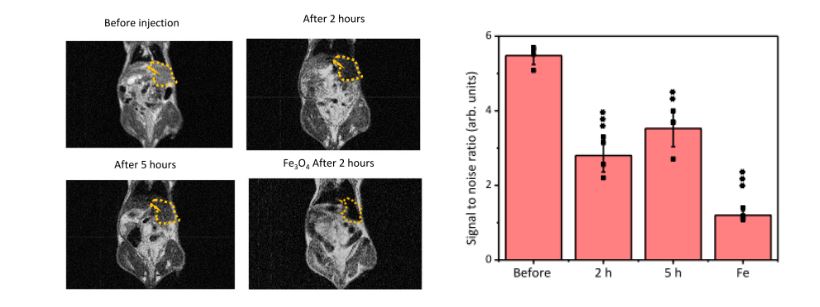
图注:[ Fig. 4:In vivo T2 – weighed MRI and NIR – II PAI (活体双模态成像图)]静脉注射DHBA–PPy@DSPE–PEG纳米颗粒后,小鼠肝脏区域在0.5 T核磁下呈现显著的T2变暗效应。
为了验证其活体应用潜力,团队制备了具有良好生物相容性的 DHBA–PPy@DSPE–PEG 纳米颗粒,并注射入裸鼠体内。在0.5 T的低场MRI系统下,注射2小时后,小鼠肝脏区域出现了明显的“变暗”区域(T2负对比效应),该区域的信噪比(S/N ratio)从5.5显著下降至2.8,证明了其在活体内的极佳造影效果和超强稳定性。
从0到1的突破: 首次报道了具有MRI活性的共轭聚合物纳米颗粒,打破了以往共轭聚合物只能用于光学/光声成像的局限,成功将其应用版图拓展至磁共振成像领域。
攻克稳定性难题: 完美解决了传统非金属有机自由基造影剂在体内易被还原、寿命短的致命缺陷。
极高的临床转化潜力: 完全摒弃了重金属离子,兼具高生物相容性与优异的体内成像效果,为下一代临床安全型非金属MRI造影剂的设计提供了全新范式。
在这项突破性研究中,低场核磁共振技术发挥了不可替代的核心作用。研究团队明确使用了 纽迈分析(Niumag)的0.5 T 小动物核磁共振成像系统进行了关键数据的采集。
纽迈低场核磁(0.5 T)在本研究中的核心贡献:
| 分析维度 | 核磁共振(NMR/MRI)数据支持 | 对科研的决定性意义 |
| 体外机制验证 | 精准测定不同配比下PPy纳米颗粒的 T2 弛豫时间 | 直接用数据证明了“部分络合”策略成功唤醒了PPy的造影活性,是验证材料设计的“试金石”。 |
| 活体造影评价 | 获取小鼠活体 T2加权图像及信噪比(S/N)定量数据 | 证实了该非金属造影剂在 0.5 T 这一接近临床低场强度的设备上,依然能提供极佳的对比度(S/N从5.5降至2.8)。 |
| 双模态开发 | 为MRI与NIR – II光声成像(PAI)的结合提供影像学基准 | 证明了共轭聚合物可以作为“光 – 磁”双模态诊疗平台的理想载体。 |
总结:没有精准的弛豫率测定与活体低场成像数据,就无法证实“休眠”聚合物的成功唤醒。纽迈(Niumag)低场核磁共振系统,正是透视非金属造影剂底层逻辑、见证材料学“从0到1”突破的得力科研利器!
文献来源:
Lin, Q., Yang, Y. & Shao, Z. Non – metallic T2 – MRI agents based on conjugated polymers. Nature Communications 13, 1994 (2022). https://doi.org/10.1038/s41467 – 022 – 29569 – x
电话:400-060-3233
售后:400-060-3233


返回顶部